Eurobio Onkologie
EndoPredict®: Lokale Testung
EndoPredict®
Schnell, zuverlässig und dezentral
EndoPredict ist ein Genexpressions-Test der zweiten Generation für ER-positive, HER2-negative Mammakarzinome, der speziell für den Einsatz in lokalen Pathologielaboren entwickelt wurde. Er liefert sowohl prognostische als auch prädiktive Einblicke1-3und unterstützt informierte Entscheidungen zur Chemotherapie bei hoher analytischer4und klinischer Genauigkeit.5,6
- EndoPredict ist als CE-IVD-Kit erhältlich, für den routinemäßigen Einsatz in molekularpathologischen Laboren validiert und bereits in über 30 Ländern sowie in mehr als 90 lokalen Laboren weltweit etabliert.
- Die Installation und Qualifizierung an einem neuen Standort dauert nur zwei Tage und wird vom erfahrenen Kundenservice-Team von Eurobio begleitet. Dieser Prozess gewährleistet konsistente und reproduzierbare Ergebnisse – unabhängig davon, wo der Test durchgeführt wird.
Durch die Möglichkeit lokaler Testdurchführung ermöglicht EndoPredict einen schnellen Zugriff auf die Ergebnisse – ohne Verzögerungen oder logistische Herausforderungen, die mit dem Versand von Proben ins Ausland verbunden wären.
Hohe Reproduzierbarkeit in lokalen Laboren
EndoPredict liefert konstant Ergebnisse von gleicher Qualität, unabhängig davon, welches pathologische Institut den Test durchführt – dies wurde durch zahlreiche Ringversuche belegt.7-9
Die Varianz und Genauigkeit der EndoPredict-Tests wurden anhand vordefinierter Referenzwerte bestimmt.
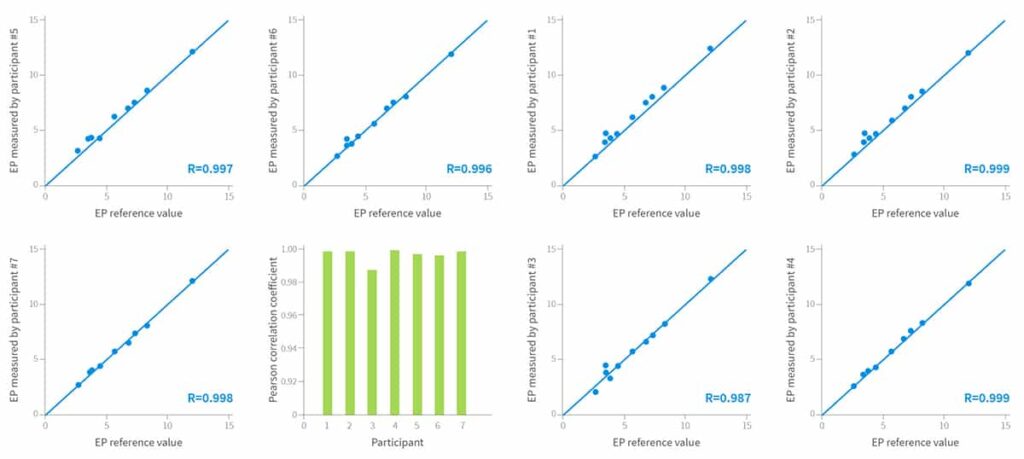
Die Evaluierung des Assays in sieben verschiedenen molekularpathologischen Laboren in Deutschland, Österreich und der Schweiz8 zeigte:
- Außergewöhnliche Übereinstimmung mit den Referenzwerten – mittlerer Pearson-Korrelationskoeffizient r= 0.996
- Alle Proben wurden der korrekten EndoPredict-Risikogruppe zugeordnet, was zu folgendem Ergebnis führte:
- Sensitivität und Spezifität von 100%
- Konkordanz von 100%
- Kappa von 1.0
Ergebnisse der dezentralen Messung von 70 Tumorproben aus zehn verschiedenen Tumoren7
Flexible Testung - Chirurgische Proben und Biopsien
EndoPredict ist für die Anwendung sowohl an chirurgischen Tumorproben als auch an diagnostischen Biopsien validiert und gewährleistet so maximale Flexibilität in der klinischen Praxis. Dies ermöglicht es, zu unterschiedlichen Zeitpunkten im Behandlungsverlauf verlässliche prognostische und prädiktive Informationen zu erhalten – sei es vor der Operation, um individuelle Therapieoptionen frühzeitig mit Patientinnen zu besprechen, oder nach der Operation, um die adjuvante Therapieplanung zu unterstützen.
Ein Vergleich der Testergebnisse zwischen Kernbiopsien und den entsprechenden chirurgischen Brustkrebsproben, bei dem der Einfluss biopsispezifischer Gewebeschädigungen auf das Testergebnis untersucht wurde, zeigte eine hohe Korrelation zwischen den gepaarten Proben. Der molekulare Score war zwischen Biopsien und Tumorproben stark korreliert (r = 0,92), und die Übereinstimmung bei der auf EndoPredict basierenden Risikoklassifikation war ausgezeichnet (Gesamtübereinstimmung 95 %, k = 0,89).10
Bei der Testung beider Probentypen liefert EndoPredict konsistente, hochwertige Ergebnisse mit der bewährten analytischen und klinischen Genauigkeit.
EndoPredict® Testung - schnell, lokal, zuverlässig
Der EndoPredict-Test zur Prognose des Brustkrebsverlaufs und zur Vorhersage des Nutzens einer Chemotherapie wird in zertifizierten lokalen Laboren durchgeführt und liefert verlässliche Ergebnisse bereits nach wenigen Tagen.
Ärzt:innen können EndoPredict leicht über ein breites Netzwerk durchführender Labore anfordern.
Über den unten stehenden Link können Sie ein lokales Labor finden und Ihre Bestellung aufgeben. Haben Sie Fragen? Wenden Sie sich jederzeit an uns - wir sind für Sie da.

EndoPredict® Test in Ihrem Labor
EndoPredict ist als CE-gekennzeichneter IVD-Kit erhältlich, der in lokalen molekularpathologischen Laboren nach einer umfassenden Vor-Ort-Schulung, die von Eurobio Scientific angeboten wird, durchgeführt werden kann.
Sind Sie daran interessiert, EndoPredict in Ihrem Labor anzubieten? Verwenden Sie das untenstehende Kontaktformular - wir werden die Anforderungen gemeinsam prüfen.
Referenzen
- Filipits M. et al.: Ein neuer molekularer Prädiktor für Fernrezidive bei ER-positivem, HER2-negativem Brustkrebs ergänzt herkömmliche klinische Risikofaktoren um unabhängige Informationen. Clin. Cancer Res. 2011
- Sestak I. et al.: Vorhersage des Nutzens einer Chemotherapie durch EndoPredict bei Patientinnen mit Brustkrebs, die eine adjuvante endokrine Therapie plus Chemotherapie oder nur eine endokrine Therapie erhalten haben. Breast Cancer Res Treat. 2019
- Filipits M. et al.: Vorhersage des Fernrezidivs mittels EndoPredict bei Frauen mit ER+, HER2-, nodalpositivem und nodalnegativem Brustkrebs, die nur mit endokriner Therapie behandelt wurden. Clin Cancer Res. 2019
- EndoPredict® QS für QuantStudio™ 5 Dx Gebrauchsanweisung Version DE/03 2025
- Buus R. et al.: Comparison of EndoPredict and EPclin with Oncotype DX Recurrence Score for Prediction of Risk of Distant Recurrence After Endocrine Therapy. J Natl Cancer Inst. 2016
- Sestak I. et al.: Vergleich der Leistungsfähigkeit von 6 prognostischen Signaturen für Östrogenrezeptor-positiven Brustkrebs. A Secondary Analysis of a Randomized Clinical Trial. JAMA Oncol. 2018
- Kronenwett R. et al.: Dezentrale Genexpressionsanalyse: analytische Validierung des genomischen Multianalysetests EndoPredict zur Brustkrebsprognose. BMC Cancer. 2012
- Denkert C. et al.: Dezentrale Genexpressionsanalyse bei ER+/Her2- Brustkrebs: Ergebnisse eines Ringversuchsprogramms für den EndoPredict Assay. Virchows Arch. 2012
- Lehmann-Che J. et al.: Erste französische Pilot-Qualitätsbewertung des EndoPredict-Tests für das frühe luminalen Mammakarzinom. Anticancer Res. 2018
- Muller B. M. et al.: Der EndoPredict Genexpressions-Assay in der klinischen Praxis - Leistungsfähigkeit und Auswirkungen auf klinische Entscheidungen. PloS ONE. 2013